甘 甜, 张凯莉, 叶 科, 刘 颖, 武书彬, 庄军平
(华南理工大学 制浆造纸工程国家重点实验室,广东 广州 510640)

1.1 原料、试剂和仪器
甘蔗渣,由广州美一食品有限公司提供。CuCl2(质量分数99.5%)、ZnCl2(质量分数99.5%)、NaBH4(质量分数98%)、 5-羟甲基糠醛(5-HMF)、 2,5-二羟甲基呋喃(BHMF)、无水乙醇、硝酸银、磷酸,均为市售分析纯;
乙腈,色谱纯;
去离子水、超纯水,实验室自制。
Parr 5500型高温高压反应釜,美国Parr公司;
Agilent 1200型高效液相色谱(HPLC)仪、电感耦合等离子体原子发射光谱(ICP-OES)仪,美国Agilent公司;
D8 Rigaku 9000型X射线衍射(XRD)仪,德国Bruker公司;
Merlin型高分辨场发射扫描电子显微镜(SEM),德国蔡司公司;
Tecnai G2 F20型透射电子显微镜(TEM),美国FEI公司;
Thermo Scientific Kα X射线光电子能谱(XPS)仪,美国赛默飞公司;
ASAP 2020 HD 88比表面积和孔隙率分析仪,美国Micromeritics公司。
1.2 催化剂的制备
参考文献方法[17-19],将甘蔗渣粉末在450 ℃的N2气氛下炭化1.5 h,得到炭化蔗渣(CBD)。以CBD作为载体,通过浸渍还原法进一步制备炭化蔗渣负载的锌和铜纳米颗粒催化剂(Cu-Zn/CBD)。分别准确称取0.8 g CBD、 0.216 mmol ZnCl2、 0.583 mmol CuCl2和60 mL去离子水于烧瓶中,剧烈搅拌2 h后,将100 mL的1%NaBH4溶液逐滴添加到烧瓶中,继续将混合物剧烈搅拌4 h。然后过滤,并将得到的混合物用去离子水洗涤,直到无氯离子被AgNO3溶液检测出来,即得到Cu-Zn/CBD。最后,将Cu-Zn/CBD在真空干燥箱中于60 ℃下干燥过夜。
1.3 HMF催化转移加氢制备BHMF
在50 mL Parr 5500型高温高压反应釜中,加入一定量的HMF、乙醇和一定量的催化剂Cu-Zn/CBD,并用N2净化反应釜5次,再充入一定的N2保持反应压力为0.5 MPa。然后加热至目标温度,在一定的反应温度(120~180 ℃)、转速300 r/min、一定的反应时间(1~4 h)条件下进行反应。反应结束后,待反应釜冷却至室温,将反应后的混合液进行过滤,分离得到的固体催化剂在60 ℃下干燥过夜,以备下次使用;
所得滤液经0.45 μm有机滤膜处理后采用HPLC检测分析,样品中HMF和BHMF的含量通过基于纯化合物的外标校准曲线法得到,HMF的转化率(y1)和BHMF的产率(y2)分别按式(1)~(2)计算。
(1)
(2)
式中:x0—初始HMF的质量,g;
x1—反应后剩余HMF的质量,g;
x2—产物中BHMF的质量,g;
MHMF—HMF的摩尔质量,g/mol;
MBHMF—BHMF的摩尔质量,g/mol
1.4 分析表征
1.4.1XRD分析 使用D8 Rigaku 9000型XRD仪,在管电压40 kV和管电流40 mA下,以Cu Kα射线为辐射源。扫描范围(2θ)为10~80°,步长0.02°,扫描速率5(°)/min,对催化剂的晶相结构进行分析。
1.4.2表面形态及结构分析 通过SEM和TEM对催化剂的表面形态及结构进行表征。
1.4.3元素分析 在具有Al Kα源(1 486.6 eV)的XPS仪上进行分析。每个光谱的结合能都用284.6 eV的C1s光谱进行校准,催化剂中锌和铜的含量采用ICP-OES测定。
1.4.4孔结构分析 BET比表面积通过ASAP 2020 HD 88比表面积和孔隙率分析仪在液氮温度下的N2吸附-脱附等温线测量,样品在N2吸附前在100 ℃的真空中脱气4 h。
1.4.5产物分析 反应结束后未反应的HMF和产物BHMF的分析检测采用安捷伦系列的液相色谱仪。产物经反相C18柱(200 mm×4.6 mm)分离,检测波长分别为284和220 nm,流动相为体积比70 ∶30 色谱纯的乙腈与质量分数0.1%磷酸水溶液,流速为0.8 mL/min,柱温保持在30 ℃,进样量为10 μL,检测时间为15 min。
2.1 催化剂表征
2.1.1BET和元素分析 表1总结了蔗渣、CBD、Cu-Zn/CBD-0(新鲜)和Cu-Zn/CBD-5(使用5次)催化剂的元素组成和比表面积(BET)。从表1可以看出,蔗渣主要由C、H和O组成。经过炭化处理后,蔗渣中的H和O含量显著降低,说明在炭化过程中发生了H和O的损失。通过ICP-OES检测,Cu-Zn/CBD-0的锌和铜纳米颗粒的质量分数分别为2.52%和1.56%,略低于理论值3.33%和1.67%,说明催化剂制备过程中,负载金属铜和锌发生了微量的损失。蔗渣、CBD、Cu-Zn/CBD催化剂的比表面积分别为9.65、 11.30和10.90 m2/g。蔗渣炭化处理后,比表面积微微增加,推测是形成的孔洞结构提高了其比表面积;
Cu和Zn纳米颗粒负载后,CBD的比表面积略微减小,但没有明显变化,推测是金属颗粒占据了小部分的孔洞结构,造成比表面积的减小。综上可以看出金属纳米颗粒的负载并未对CBD的多孔结构产生较大影响。

表1 不同样品的元素组成和比表面积Table 1 Element composition and surface area of different samples
2.1.2SEM和TEM分析 使用SEM和TEM对CBD、Cu-Zn/CBD(新鲜)和Cu-Zn/CBD(使用5次)的表面形貌、结构特征及铜锌金属的分布情况进行了分析,结果如图1所示。

a.CBD, SEM; b.Cu-Zn/CBD- 0, SEM; c.Cu-Zn/CBD-5, SEM; d.Cu-Zn/CBD- 0, TEM; e.Cu-Zn/CBD-5,TEM图1 不同样品的SEM和TEMFig.1 SEM and TEM images of different samples
从图1(a)可以看出,CBD中存在一些孔洞结构;
且催化剂的结构与载体相似,这表明负载金属Cu、Zn的过程中并未对CBD的表面微观结构产生较大影响。观察图1(b)可以发现金属元素的存在,金属颗粒已经较为均匀地负载到了载体表面,但在图1(c)中可以看到金属颗粒发生了轻微的团聚现象。此外,为了研究Cu和Zn纳米颗粒的分布和尺寸,通过TEM对Cu-Zn/CBD催化剂进行了表征,如图1(d)、(e)所示,与图1(b)的分析结果一致,即金属纳米粒子已经被成功地负载到了载体上,且分散度较高。Cu-Zn/CBD催化剂的TEM图像表明这些纳米颗粒的尺寸约为4 nm。
2.1.3XRD分析 图2为CBD、Cu-Zn/CBD(新鲜)、Cu-Zn/CBD(使用5次)和Cu-Zn/CBD(再生)的XRD谱图。从图2可以看出,在2θ为20~30°之间出现了宽而明显的衍射峰,该衍射峰对应无定形炭的特征峰,说明CBD形成了无定形炭结构。对比图2中a、b、c和d的谱线可以发现,这些样品的XRD谱图没有太大差异,说明Cu-Zn/CBD催化剂在铜、锌金属的浸渍负载过程中并没有改变CBD的基本结构。

a.载体support(CBD); b.新鲜fresh; c.使用5次used 5th; d.再生regenerated图2 载体和不同状态催化剂的XRD谱Fig.2 XRD patterns of support and catalysts in different states
2.1.4XPS分析 用XPS分析了Cu-Zn/CBD的表面元素组成,结果如图3所示。结合能分别为284.6和532.6 eV的峰依次对应C1s,O1s的特征峰,这证实了Cu-Zn/CBD催化剂存在C和O元素。此外,还观察到结合能分别为933.2和1 022.2 eV 的峰,这表明Zn、Cu纳米颗粒被负载在载体上。为了进一步了解催化剂表面Cu、Zn纳米颗粒的状态,对Cu、Zn纳米颗粒的XPS谱图进行了高分辨率扫描。从Cu2p的高分辨率XPS谱图中可以看出,在954.5和933.1 eV结合能处出现了2个强峰,分别对应于Cu2p3/2和Cu2p1/2。同时,在Zn2p的高分辨XPS谱图中观察到2个分别位于1 045.1和1 022.2 eV结合能处的强峰,这2个峰分别对应于Zn2p3/2和Zn2p1/2。以上结果表明:Cu、Zn以零价态的形式负载到催化剂的表面。

图3 Cu-Zn/CBD的XPS总谱(a)及Zn2p(b)、Cu2p(c)的分峰结果Fig.3 XPS spectrum of Cu-Zn/CBD(a) and peak separation results of Zn2p(b),Cu2p(c)
2.2 反应条件对5-羟甲基糠醛氢化的影响
2.2.1催化剂金属比例的影响 研究了不同催化剂金属质量比对HMF加氢的影响,以进一步研究Zn和Cu纳米粒子之间的协同效应,结果见表2。所有实验均在固定的反应条件下进行,反应条件为0.1 g HMF,在25 mL乙醇、 0.15 g催化剂、 0.5 MPa N2、 160 ℃下反应2 h。由表2可知,当只有CBD作用时,HMF只发生极其微弱的转化。在单独使用Cu/CBD催化剂的情况下,HMF的转化率为70.6%,而BHMF的产率只有36.2%。单金属催化剂Zn/CBD的HMF转化率仅为21.0%,但是当使用Cu-Zn(1 ∶1)/CBD时,HMF转化率为79.1%。当使用Cu-Zn(2 ∶1)/CBD时,HMF转化率为89.0%,BHMF的产率为83.0%;
相比之下,当使用Cu-Zn(1 ∶2)/CBD作为催化剂时,HMF转化率仅为16.9%。可以看出,Cu和Zn纳米颗粒对HMF的氢化具有重要影响,并且双金属纳米颗粒的存在对整个催化加氢反应有较好的催化效果。综合实际催化效果等各方面因素,选择Cu-Zn(2 ∶1)/CBD催化剂最合适。

表2 催化剂金属质量比对HMF氢化的影响Table 2 Effect of catalyst metal mass ratio on catalytic hydrogenation of HMF
2.2.2反应温度的影响 反应温度对HMF加氢反应的影响如图4(a)所示。
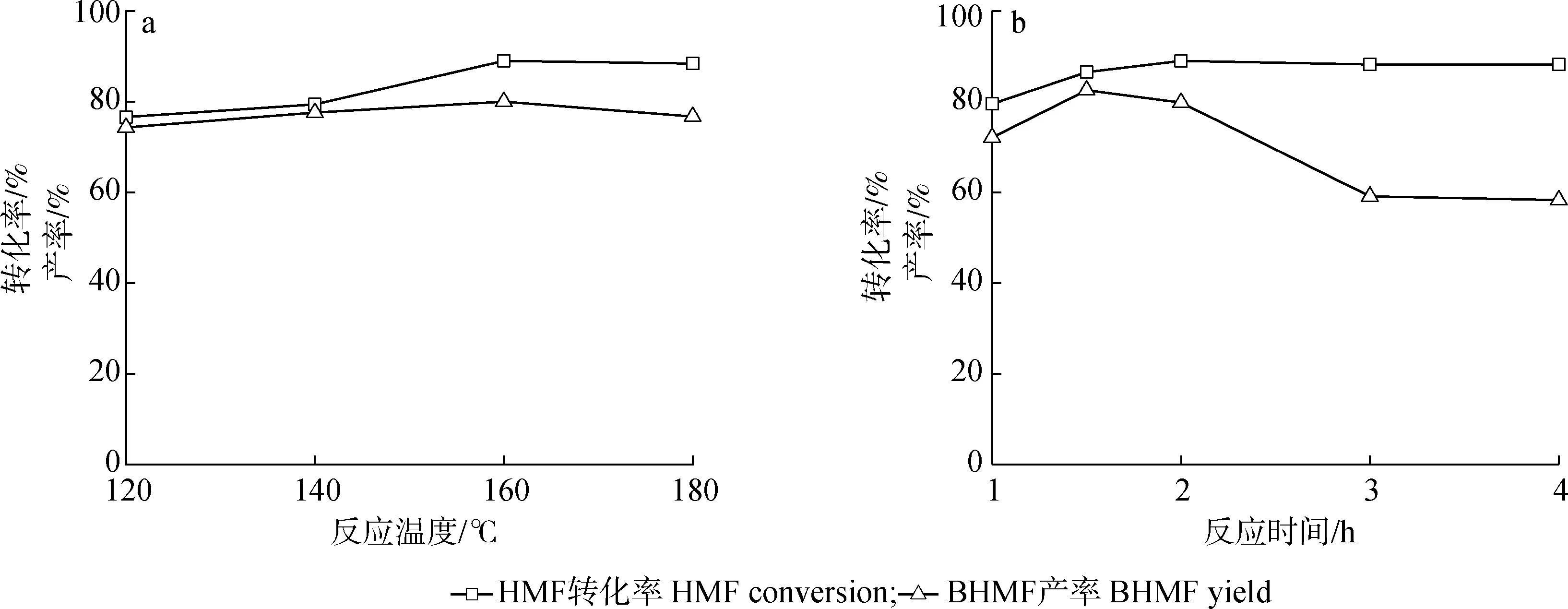
图4 反应温度(a)和反应时间(b)对HMF氢化的影响Fig.4 Effect of reaction temperature(a) and reaction time(b) on HMF hydrogenation
由图4(a)可知,在使用Cu-Zn/CBD(0.15 g)将HMF选择性氢化为BHMF的反应中反应湿度起着重要作用。反应时间为2 h,通过将反应温度从120 ℃提高到160 ℃,HMF转化率从76.6%提高到89.0%。当反应温度进一步提高时,HMF转化率几乎保持不变。同时,随着反应温度从120 ℃增长到160 ℃,BHMF的产率从74.3%上升到80.0%,而当温度继续升高到180 ℃时,产率下降到76.7%,推测温度过高时,生成的BHMF容易进一步氢化形成其他加氢产品,如2,5-二甲基四氢呋喃(DMTHF)、 2,5-二甲基呋喃(DMF)等。因此,最佳的反应温度为160 ℃。
2.2.3反应时间的影响 探索了在160 ℃下,不同反应时间(1、 1.5、 2、 3和4 h)对HMF转化为BHMF的影响,结果如图4(b)所示。由图可知,通过将反应时间从1 h延长到3 h,HMF的转化率从79.5%增加到88.2%,在3 h后HMF转化率几乎保持不变;
同时,BHMF的产率在1到1.5 h内有明显的增加,从72.1%上升到82.5%,而当反应时间延长到4 h时,产率下降到58.3%,推测随着时间的延长BHMF选择性的降低主要由于BHMF的过度氢化导致。综合考虑,选择反应时间为1.5 h较为适宜。
2.3 主要反应途径
HMF分子包含一个醛基、一个醇羟基和呋喃环,因此HMF在催化剂和氢供体的存在下易于被氢化形成多种产物[20-21]。HMF分子中的醛基和醇羟基分别氢化生成BHMF和5-甲基糠醛(5-MF)。BHMF和5-MF能够进一步氢化形成5-甲基糠醇(MFA),然后MFA最终氢化形成DMF[22-24]。在前人研究的基础上,总结了Cu-Zn/CBD催化HMF氢化转化得到BHMF的可能反应途径,如图5所示。
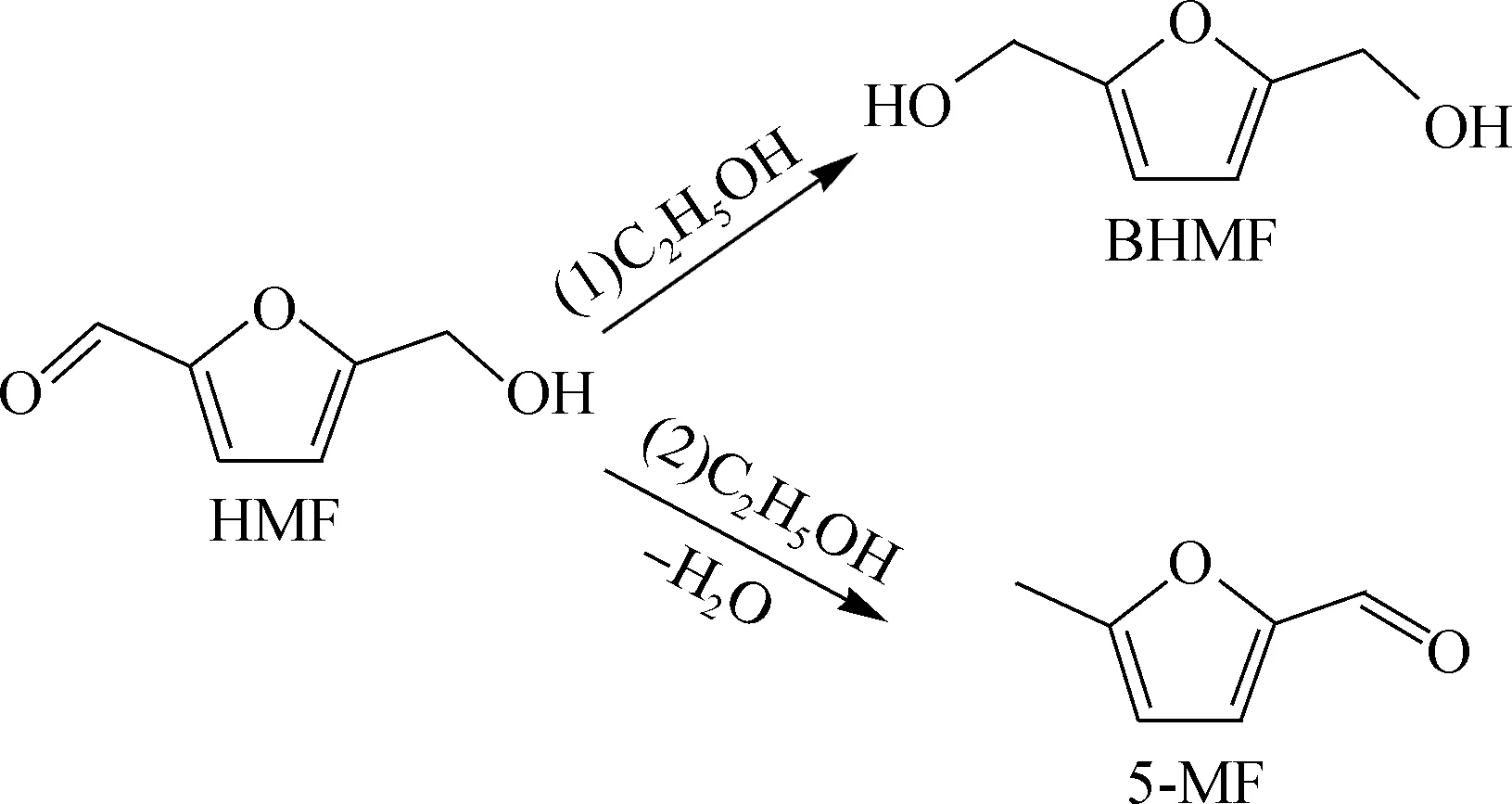
图5 HMF转化为BHMF的反应途径Fig.5 Reaction pathway of HMF into BHMF
2.4 催化剂的重复使用性能
催化剂的高效稳定性和可重复使用性对于BHMF的实际生产具有重要意义,在最优反应条件下通过Cu-Zn/CBD催化剂的循环实验来考察催化剂的稳定性。在每次的循环实验中,反应完成后,催化剂经过滤从反应混合物中分离出来,然后用水清洗并在真空干燥箱中干燥过夜,然后再循环使用[25,13]。从表3可以看到,催化剂使用5次后催化性能有较明显的下降,HMF转化率和BHMF产率均有所下降。可能是因为HMF加氢制备的BHMF及其他副产物附着在催化剂表面和孔洞结构中,从而阻碍了反应物HMF、氢供体乙醇与催化剂的活性位点相接触,最终导致乙醇的氢解速率减慢,HMF的加氢速率也减慢,表现为催化剂的性能下降。同时,结合前文的TEM图像(图3(e))中观察到少量的Cu和Zn纳米颗粒发生了聚集现象,这可能导致催化剂发生了轻微失活;
而ICP-OES检测了使用5次后的催化剂中的铜和锌物种含量(表1),结果表明金属损失是催化剂活性降低的原因。

表3 使用次数对催化剂催化活性的影响Table 3 Effect of use times on catalytic activity of catalyst
3.1XRD分析表明Cu-Zn/CBD催化剂在Cu、Zn金属的浸渍负载过程中并没有改变CBD的基本结构;
XPS、SEM和TEM分析,以及元素分析结果都表明活性金属Cu、Zn成功负载于催化剂表面,且以零价的形态均匀分布在CBD上;
BET分析表明铜和锌纳米颗粒负载后,CBD的比表面积变化不大,进一步说明了金属纳米颗粒的负载并未对CBD的结构产生较大影响。
3.2Cu-Zn/CBD催化剂在催化HMF制备BHMF的反应中表现出较高的活性,在乙醇为氢供体和反应溶剂,Cu/Zn质量比为2 ∶1,反应温度为160 ℃,反应时间为1.5 h的最佳反应条件下,HMF的转化率为86.5%,BHMF的产率为82.5%。
3.3Cu-Zn(2 ∶1)/CBD催化剂的重复使用性能较好,重复使用5次后,金属活性位点与底物和乙醇无法充分的接触,乙醇的氢解速率及HMF的加氢速率随之减慢,HMF转化率下降为77.3%,BHMF产率下降为76.8%。
猜你喜欢氢化产率转化率我国全产业领域平均国际标准转化率已达75%机械工业标准化与质量(2022年6期)2022-08-12污水厂污泥产率随季节变化研究城市道桥与防洪(2022年3期)2022-05-08α-烷基苯乙酰胺的合成新方法合成化学(2021年5期)2021-06-04CeCl3和CeO2对松木屑的催化热解作用研究安全与环境工程(2021年2期)2021-04-02原煤深度解离分步释放浮选试验研究煤炭加工与综合利用(2020年6期)2020-07-17钽锭氢化工艺的研究中国金属通报(2020年4期)2020-07-04一种多孔钛膜专用钛粉末或钛合金粉末的制备方法钛工业进展(2020年6期)2020-01-05曲料配比与米渣生酱油蛋白质转化率的相关性中国调味品(2017年2期)2017-03-20氢化锆的使用性能研究现状科技传播(2016年17期)2016-10-10透视化学平衡中的转化率中学化学(2015年2期)2015-06-05