蔡春雨,何凤珍,余电有,,何斌,权里平,言纬,张震,韦勤将,黄显南,刘莉,
(1. 右江民族医学院研究生学院,广西 百色 533000;
2. 右江民族医学院附属医院心血管内科,广西 百色 533000)
心房颤动(atrial fibrillation,AF)是临床上最常见的快速心律失常之一,其特点是左心室或双心室扩张和收缩受损,是心力衰竭和心源性猝死的重要原因,其发生率和患病率均呈上升趋势,大大增加了住院率、中风发生率、社会医疗负担和生活质量[1-3]。虽然目前AF有多种治疗方法,但其发病机制尚不清楚。目前,全基因组关联研究(GWAS)已经发现了超过100个与AF相关的基因位点,其中大多数位点指向离子通道、独特的心脏富集转录因子以及其他调控基因[4-5]。心脏动作电位是通过多种离子通道的协同活动产生和传播的,Nav1.5与肌细胞膜内的Navβ亚基和其他调控蛋白形成大分子复合物,其中主要的心脏亚型Nav1.5由SCN5A编码,β1和β1b由SCN1B编码,以维持正常的心脏功能,Nav复合体紊乱可表现为致死性心律失常[6]。目前,关于心脏钠通道基因(SCN5A)、钠离子通道β1亚基(SCN1B)在人类AF中的作用有部分相关报道,但在广西少数民族地区分布特征少有报道,因此本研究旨在探讨SCN5A、SCN1B基因SNPs位点与房颤间的关联性,及与不同地区种族人群相比较,以期呈现AF遗传学的现状及其可能潜在的临床应用。
1.1 数据收集 收集所有入组患者一般临床指标,并详细询问其家族史、高血压史、糖尿病史、心脏病等病史并记录,通过24 h动态心电图或12导联心电图检测确定诊断为AF的患者,同时通过心电图或超声心动图明确诊断,排除有严重器质性心脏病和有心脏病家族史等。
此外,对其禁食12 h后用EDTA采集外周静脉血5 mL,提取DNA,测定生化指标。
1.2 SCN5A、SCN1B SNPs检测 DNA提取步骤由华大公司提供的QIAamp DNA Micro提取试剂盒,严格依照说明书操作。将所有提取得到的DNA送到武汉华大公司完成DNA测序,测序得到病例组中SCN5A、SCN1B的特异的核苷酸变异(SNV),分别在NCBI、Ensembl、千人基因组数据库等中进行序列比对,筛选出新突变位点,采用PCR扩增,首先在PubMed查询SCN5A、SCN1B的基因序列,利用Primer Premier 5.0软件设计各位点引物,委托华大基因科技有限公司合成,并建立PCR扩增反应体系,对PCR扩增产物进行SNPs基因分型,提纯后的产物再使用Sanger测序方法对相应样本的突变位点进行验证,经Chromas软件处理后获得对比后的测序峰图,最后将不同突变位点与不同数据库对比,分析基因型及等位基因发生频率以及可能致病风险评估。
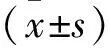
2.1 AF组和对照组一般资料比较 本研究选取广西地区105例AF样本[平均年龄(67.25±11.96)岁,男性62.86%],通过24 h动态心电图或12导联心电图检测确定诊断,同时纳入同一地区105例健康人样本为对照组[平均年龄(58.42±12.04),男性56.19%],同样有严重器质性心脏病和有心脏病家族史的样本均排除在外。其中,年龄在AF组高于对照组,差异有统计学意义(P<0.05),见表1。本研究方案和外周静脉血的收集均经当地伦理委员会和右江民族医学院附属医院医学伦理委员会批准[伦研批第(YYFY-LL-2016-001)号],受试者或其家属均签署知情同意书。
2.2 样本SNP位点确认及核苷酸序列分析 通过对SCN5A、SCNB基因测序及筛选发现SCN5A基因上3个多态性位点,分别是rs1805124(H558R)、rs1805125(P1090L)、rs41261344(R1193Q);
发现SCN1B基因3个位点分别是rs55742440(L210P)、rs67701503(S248R)、rs67486287(R250T)。本课题组提取了携带以上位点样本的基因组DNA,进行Sanger测序验证,设计引物,见表2。其中SCN1B 基因rs55742440、rs67701503、rs67486287的3个位点距离相近,因此设计共同的上下游引物(F4:5′-CATTGAGGTAGTGGACAAAG-3′,R4:5′- GAGAAACACATCGGATTATTATC-3′)。测序结果以上6个位点PCR产物测序峰图,见图1。

表1 AF组与对照组一般资料比较

表2 SCN5A各个多态性位点所用引物

A1~A3分别为SCN5A基因rs1805124、rs180512、rs41261344位点基因型验证分析;
B1~B3分别为SCN1B基因rs55742440、rs67701503、rs67486287位点基因型验证。图1 SCN5A和SCN1B基因SNPs位点的Sanger测序图谱
2.3 SCN5A、SCN1B基因的SNPs在AF组和对照组中的分布 SCN5A基因rs1805124、rs1805125、rs41261344位点的等位基因和基因型频率均符合Hardy-Weinberg 平衡。rs1805124位点存在3种基因型:TT、TC、CC;
与携带TT基因型的研究对象相比,CC 基因型患AF风险OR值为1.283(95%CI:0.084~19.595),TC基因的OR值为4.147(95%CI:0.303~56.800),相对于T等位基因,C等位基因的增加AF罹患风险OR值为0.302(95%CI:0.127~0.717,P=0.007)。rs1805125存在3种基因型:GG、GA、AA,该位点为罕见突变体,其GG、GA、AA基因型在两组分布差异无统计学意义(P>0.05),等位基因G、A分布差异无统计学意义(P>0.05)。rs1805124、rs41261344位点的基因型及等位基因频率在AF组和对照组中差异有统计学意义(P<0.05),见表3。SCN1B基因rs55742440、rs7701503、rs6748-6287位点的等位基因和基因型频率均符合Hardy-Weinberg平衡,同时以上3个位点的基因型及等位基因频率在AF组和对照组中差异无统计学意义(P<0.05),见表4。

表3 SCN5A基因SNP在AF组和对照组的分布

表4 SCN1B基因SNP在病例组和对照组的分布
2.4 本地区AF组和其他地区人群SCN5A、SCN1B基因SNPS多态性位点基因型频率和等位基因频率比较 SCN5A基因rs1805124、rs41261344的基因型及等位基因频率在少数民族地区人群AF组和其他地区人群中差异有统计学意义(P<0.05)。rs1805125位点各个基因型、等位基因在少数民族地区AF组与东亚地区AF组中差异无统计学意义(P>0.05),而等位基因频率在少数民族地区 AF 组与全球、非洲、欧洲、南亚、美洲AF组中差异有统计学意义(P<0.05)。见表5~表7。SCN1B基因rs55742440、rs67701503、rs67486287位点基因型、等位基因在少数民族地区AF组与东亚地区AF组中差异无统计学意义(P>0.05),与全球、非洲、欧洲、南亚、美洲AF组中差异有统计学意义(P<0.05)。见表8~表10。

表5 本地区AF人群SCN5A基因rs1805124与其他地区人群分布比较

表6 本地区AF人群SCN5A基因rs1805125与其他地区人群分布比较

表7 本地区AF人群SCN5A基因rs41261344与其他地区人群分布比较

表8 本地区AF人群SCN1B基因rs55742440与其他地区人群分布比较

表9 本地区AF人群SCN1B基因rs67701503与其他地区人群分布比较

表10 本地区AF人群SCN1B基因rs67486287与其他地区人群分布比较
心脏动作电位是由多个离子通道协同激活形成的,其中钠离子通道成孔的α亚基与调节其表达和功能的β亚基相结合[7-8]。最早OLSON T M等[9]发现遗传性SCN5A错义突变与早发性扩张型心脏病和AF易感性相关。随后OLESEN M S等[10]在192例早发性单纯性AF患者中发现SCN5A的8个突变和2个罕见变异,经电生理研究发现这些突变表现出重叠的功能效应,导致瞬时峰值电流减弱和持续电流增加,表明心脏INa电流增加或功能丧失改变都构成了早发性房颤的底物,提示SCN5A是构成早发性房颤的可能基质。同样,WILDE A A M等[11]发现SCN5A基因突变改变了钠通道功能,导致钠内流进一步减少,动作电位持续时间缩短,进而导致心律失常。综上所述,INa电流受损不仅促进AF,还会引起其他一些心律失常,如病态窦房结综合征(SSS)、长QT综合征(LQT)、早期复极综合征(ERS)、Brugada综合征(BrS)[12]。
NaV β亚基有5种亚型(β1~β4和β1b),Navβ1~β4是跨膜蛋白,而Navβ 1b是一种发育调节的分泌蛋白,分别由SCN1B-SCN4B编码,在人心脏中最丰富的亚型是NaV1.5和β1亚基[12-13]。研究表明[14]Navβ亚基早期被发现可促进Nav通道复合物的细胞表面表达,导致电流密度的增加。而与BrS相关的SCN1B突变是第一个被发现的与心脏相关的,该突变具有引起心室纤颤(ventricular fibrillation,VF)心脏性猝死的高风险[15]。随后,WATANABE H等[16]在AF患者中发现了SCN1B β亚基基因非同义突变(R85H、D153N),与野生型-亚基共表达相比,突变体降低了钠电流峰值幅值,对SCN5A介导的电流产生功能丧失的影响,这些发现进一步支持了Na电流降低增强AF易感性的假说。最近研究表明,Navβ1和Navβ3变异通过调节Nav1.5的表达和门控特性来促进AF和BrS的发生,但二者机制不同[6]。
本研究结果发现AF组平均年龄高于对照组,提示年龄是AF的独立危险因素。通过基因测序发现了SCN5A基因rs1805124、rs1805125、rs41261344 3个位点的基因型,并且AF组基因型和等位基因分布与对照组之间差异有统计学意义。其中,最早研究发现,SCN5A基因rs1805124多态性与美国孤立性房颤相关[17]。同样,单丽沈等[18]于2012年研究发现SCN5A基因rs1805124与高海拔藏汉民族房颤的发生有关。随后又被报道该位点在新疆汉族和维吾尔族房颤患者中存在民族差异,G等位基因是AF的独立危险因素[19-20]。而本研究结果也显示TC和CC基因型是AF最常见的基因型,C等位基因是AF的独立危险因素,与其他研究结果不一致,提示C等位基因可能是另一易患基因。BrS是一种主要由SCN5A变异引起的遗传性心脏性猝死疾病,在亚洲人群中更为普遍.其中SCN5A 基因rs1805125、rs41261344位点常见于长QT综合征和Brugada综合征患者[21]。研究表明[22],P1090L变体可能会对Nav1.5产生功能性影响,但可能不会导致二次结构变化,其功能效应取决于与Q1077剪接变异体的相互作用,R1193Q变异可能影响Nav1.5的二级结构,并增加BrS中致命性心律失常的易感性。然而,对于R1193Q位点与心律失常的联系仍在争论中,ABE M等[23]研究表明R1193Q不会调节NaV1.5通道以响应体温变化,其可能不是触发心律失常的单基因因素。本研究结果发现SCN5A基因rs1805125位点在AF组等位基因分布与对照组之间差异无统计学意义,并且该位点在东亚AF患者中无差异。rs41261344在AF组中CT基因型及T等位基因频率高于对照组,表明T等位基因可能是AF的易患基因。
既往研究已证明,SCN1B可以增强SCN5A通道(a亚单位)传导的钠通道电流[24]。HU D等[25]首次证明Navβ1B亚基与Nav1.5和Kv4.3在结构和功能上存在关联,并且该亚基的罕见R214Q位点遗传变异通过同时减少内向电流(INa)和增加外向电流(Ito),从而调节负责BrS和心源性猝死的致心律失常底物。而具有相同SCN5A突变的患者的表型是可变的,因为各种修饰物可能会对其进行调节。AOKI H等[26]在携带相同SCN5A突变的家族成员中发现了不同表型,并在先证者、其母亲和妹妹体内检测到SCN1B-L210P,考虑其可能作为影响表型的遗传修饰物。SCN1B的变异也与AF和心脏传导功能障碍有关[16]。YAO H等[27]在4个早期复极综合征家族中发现SCN1Bβ基因的S248R和R250T突变,其与Kv4.3相关,导致Ito增加,考虑可能作为ERS调控基因之一。由于本研究rs55742440、rs7701503、rs67486287位点的高等位基因频率和在人群中携带该变体的高纯合子数,并且在对比东亚AF人群基因型和等位基因频率人群分布差异均无统计学意义,故考虑其为良性变异且无有害性。综上,疾病的表型受到突变、遗传背景和环境之间的相互作用,是一个互相影响的复杂过程。
AF复杂遗传学的揭示最终可能使心律失常的离散临床亚型和机制的识别成为可能。随着对AF相关遗传危险因素理解的迅速扩展,有望识别其发病机制中涉及的新途径、新药物靶点,以及特定临床结果的风险患者。本研究有一定的局限性,因样本量及入组来源较小,相关结果具有一定的局限性,因此,今后应开展更全面、样本量更大的研究,同时未来研究这些多态性位点与SCN5A、SCN1B在核酸、蛋白水平以及组织特异性之间的相关性的工作,有望阐明这些SNPs与AF的关联机制。
猜你喜欢亚基等位基因基因型亲子鉴定中Penta E稀有等位基因28的确认1例川北医学院学报(2022年6期)2022-06-24亲子鉴定中男性个体Amelogenin基因座异常1例智慧健康(2021年17期)2021-07-30心脏钠通道β2亚基转运和功能分析世界最新医学信息文摘(2020年68期)2020-12-25广东汉族人群Penta D基因座off-ladder稀有等位基因分析中国产前诊断杂志(电子版)(2020年1期)2020-05-21蓝隐藻藻蓝蛋白亚基的分离及特性研究烟台大学学报(自然科学与工程版)(2020年1期)2020-02-08贵州汉族人群23个STR基因座的OL等位基因研究遵义医科大学学报(2020年6期)2020-02-05上海郊区牛病毒性腹泻病毒(BVDV)基因型分析上海农业学报(2017年3期)2017-04-10作物遗传育种研究进展Ⅴ.表型选择与基因型选择作物研究(2014年6期)2014-03-01小RNA干扰蛋白酶体亚基α7抑制K562细胞增殖中国医学科学院学报(2013年6期)2013-03-11甘蔗黄叶病毒基因型研究进展中国糖料(2013年1期)2013-01-22